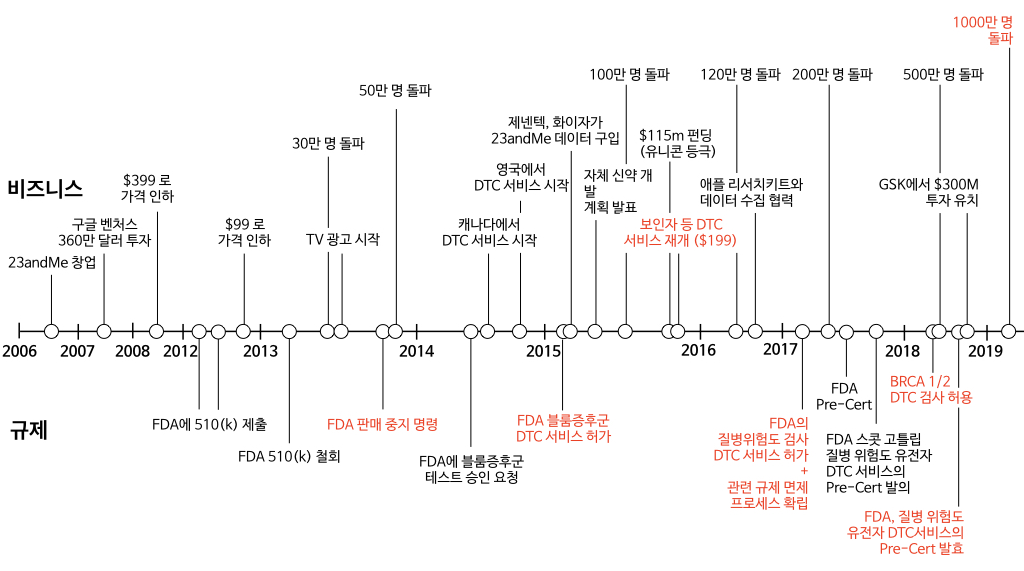
최근 하버드 비즈니스 리뷰에 23andMe의 CEO 이자 공동창업자인 앤 워짓스키의 글이 실렸다. 개인 유전 정보 분석회사 23andMe가 어떻게 FDA의 규제를 거쳐서 지금에 이르렀는지를 담담하게 회고하는 글이다. 참고로 23andMe는 기업가치 $2B 이상의 유니콘으로 천만 명 이상의 사람들이 23andMe를 통해 자신의 유전정보를 분석했다. (참고로 DTC (Direct-to-Consumer) 유전정보 서비스는 몇몇 예외를 제외하면 한국에서는 불법.)
23andMe는 개인 소비자에게 직접 유전 정보 분석 서비스를 판매하는 DTC 모델을 창업 초기부터 지금까지 고수하고 있다. 초창기에는 질병 위험도 분석, 보인자 분석 등의 민감한 분석까지 최대 $99의 저렴한 가격에 제공하면서 미국에서 선풍적인 인기를 얻었다. 그러다가 갑자기 2013년 11월에 FDA로부터 사업을 중지하라는 Letter를 받게 된다.
당시로서는 업계가 발칵 뒤집힐만한 일이었다. Letter에 실린 문구가 이례적으로 강경했고, 약간은 감정적으로도 읽힐 수 있기 때문이었다. (혹자는 ‘마치 버림 받은 옛날 연인이 보낸 편지 같다’고도 했다.) 당시에 나는 이미 23andMe를 꽤 관심있게 팔로업하고 있었고, 운 좋게도(?) 내 타액을 미국으로 보내어서 23andMe의 분석 결과를 갓 얻은지 얼마 되지 않았을 때였다.
(2013년 11월 이후로 23andMe의 분석 항목은 대폭 축소되어서, 지금까지도 그 이전의 다양한 분석 항목을 모두 제공하고 있지는 않다. 내 침을 태평양 너머로 보내는 것이 조금만 늦었더라면, 23andMe의 원래 서비스 항목을 보지 못할 뻔 했다. 덕분에 그 결과는 내 ‘헬스케어 이노베이션’과 이번 ‘디지털 헬스케어’에도 실렸다.)
앤 워짓스키는 지금 어떤 생각을 하고 있을까?
당시에 FDA가 보낸 그 Warning Letter의 원문을 읽어보니 드는 질문은 한 가지였다. ‘앤 워짓스키는 지금 어떤 생각을 하고 있을까?’ 혁신가로서 6, 7년 동안 새로운 산업을 개척해오다가, 갑자기 편지 한 통으로 그 사업이 중단될 위기에 놓여 있을 때 스타트업의 CEO로서 어떤 결정을 내리려 하고 있을까.
이번 아티클은 그 당시의 이야기가 그녀 본인의 글로 담겨져 있다. 내가 알기로 그 당시의 전후 상황에 대해서 스스로 밝혔던 적은 없었던 것 같다. 외부적으로 일어난 일은 이제 우리가 모두 알고 있지만 (심지어 내 졸저 ‘디지털 헬스케어’에는 아예 23andMe 연대기 까지 그려넣었다) 내부적으로 어떤 일이 있었는지 알 길이 없었다.
이번 아티클을 보면, 내부적으로 FDA에 항의하는 등 많은 전문가 들의 의견을 들으면서 여러 옵션을 고려했다고 나온다. FDA의 결정에 항의하며 저항하는(?) 선택지를 포함해서 말이다.
그 이후에 실제로 일어난 일은 우리가 모두 알고 있는 바다. 결국 23andMe는 정석적으로, 우직하게 정면돌파를 했다. FDA의 지시를 받아들이고, 이후 FDA와 함께 협의하면서 근거를 만들고 의료기기로서 허가를 받으며, 분석 항목을 한 번에 하나씩 늘려갔다.
FDA의 경고장을 받은 지 14개월만인 2015년 2월 블룸증후군 한 가지 종류의 질병 위험도 분석에 허가를 받은 것을 시작으로, 2017년 4월 파킨슨병 등 10가지 질병에 대한 위험도 분석 허가를 받으며 차근차근 FDA를 설득한 것이다. 그 결과 FDA의 규제 방식에도 점차 변화가 생기게 되었다. 이는 수 년이 걸렸지만, 지나고 보면 역시 그 방법이 가장 빠르면서도, 현명한 길이었던 것 같다. (그 과정에서 사내 문화나 인력구조에 대대적인 개편이 필요했다고 나온다. 결코 쉬운 일이 아니었을 것이다.)
물론 그 과정에서 질병 예측성 분석과 함께 23andMe의 또 다른 중심 비즈니스였던 조상 분석은 FDA의 금지를 받지 않았기 때문에 23andMe가 버틸 수 있던 힘이 되기도 했다. 하지만 중심 비즈니스 중의 하나가 갑자기 불가해진 상황에서 회사가 (DTC 라는) 서비스 방식을 고수하면서 수년 동안 버티고, 또 투자자도 이를 참고 기다려주는 것은 정말 어려운 일이었을 것이다. (심지어 FDA로부터 금지를 받고, 인허가를 다시 준비하던 2015년에 시리즈E 펀딩 라운드가 진행되었다. 이때 일루미나 벤처스, GV 등이 참여했다. 한국이라면 규제 받아서 서비스의 큰 부분이 정지된 회사가 새로운 투자를 받을 수 있었을까?)
규제도 결국 사람이 하는 것
이 글을 읽으며 들었던 생각은 혁신을 하려는 창업가도, 규제기관도 결국에 사람이라는 것이다. 창업가도, 규제기관도 사람이 하는 일이므로, 감정과 방향성을 가지고 있다. 최근 내가 식약처, 심평원에 전문가 협의체 등으로 자문으로 참여하면서 많이 느낀 것 역시 규제도 역시 사람이 하는 것이라는 점이다.
그들도 규제를 더 합리적으로 잘 하고 싶어하고, 본인의 맡은 역할을 더 잘 하고 싶어한다. 자기 역할을 제대로 못하고 싶은 사람은 없다. 하지만 디지털 헬스케어니 하는 것들이 나오면서, 기존의 규제 기준, 프레임워크에 잘 맞지 않고 애매한 것들이 자꾸 등장하는 것이 근원적인 문제다.
이번 아티클에서도 23andMe의 서비스가 처음 나왔을 때 FDA가 기존에 정의하던 ‘의료기기’의 기준에 해당되는지를 23andMe도 모르고, FDA도 명확하게 결론 내리기 어려웠다고 나온다. 양 기관은 오랫동안 조율을 해가는 과정에 있었으나, 그 과정에서 23andMe는 FDA의 심기를 건드렸다. (더 정확히는 FDA의 몇몇 주요 인사의 심기를 건드렸을 것이다. 정확히 이유가 무엇이었는지는 앤 워짓스키가 지금도 잘 모르겠다고 한다. 나를 포함한 외부에서는 대대적인 TV 광고 등이 이유였을 것이라고 추측하고 있다.)
이런 과정에서는 서로 이해시키고, 이해하려는 과정이 중요하다. 기존에 없던 완전히 새로운 것을 만들고자 한다면, 기존에 있던 것들을 규제하기 위해 만들어진 규제 프레임워크에 잘 들어맞지 않는 것이 일견 당연할 수밖에 없다. 결국 규제 당국과 협의하고, 설득하고, 어떨 때는 교육시키면서 나아가야 한다. 이런 과정은 지금도 진행되고 있고, 앞으로도 계속 반복될 것이다.
23andMe는 그 과정을 잘 거침으로써 지금에 이를 수 있게 되었다. 국내외 다른 디지털 헬스케어 스타트업도 그런 과정을 잘 거칠 수 있기를 기대한다. 그렇게 될 수 있도록 나도 내가 할 수 있는 역할을 열심히 하고 있다.
Discover more from 최윤섭의 디지털 헬스케어
Subscribe to get the latest posts sent to your email.